FALP responde a Mañalich: "El plasma se ha usado hace bastante tiempo en distintas pandemias"
El ministro de Salud calificó ese tratamiento en pacientes con covid-19 como "extraordinariamente riesgoso". Desde la fundación afirman que "el plasma tiene el mismo riesgo que una transfusión de sangre".
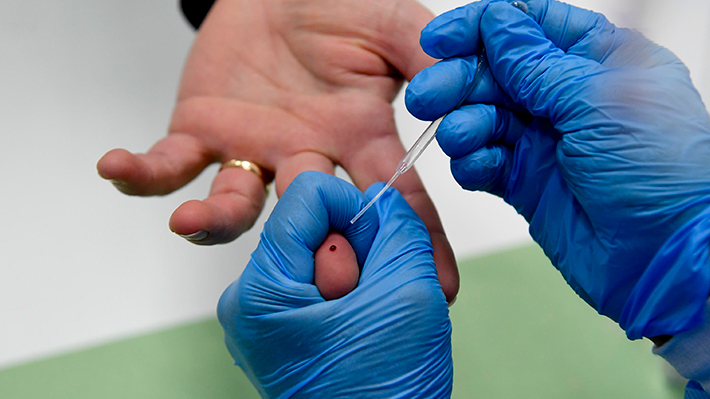
by Redactado por N. Ramírez, EmolSANTIAGO.- Uno de los tratamientos que se está probando en los casos de pacientes más graves con covid-19 es la utilización de plasma de personas que ya superaron la enfermedad. De hecho, la Fundación Arturo López Pérez (FALP) inició una campaña para que las personas convalecientes lo puedan donar.
Sin embargo, el ministro de Salud, Jaime Mañalich, calificó ese tratamiento como "extraordinariamente riesgoso" y afirmó que "no hay una autorización" ni "evidencia cierta de que sea una terapia que contribuye al manejo de los pacientes más graves".
Desde FALP respondieron al ministro y afirmaron que "el plasma tiene el mismo riesgo que una transfusión de sangre" y agregan que "hay publicaciones científicas de Estados Unidos que demuestran una reducción de la mortalidad" en pacientes con covid-19.
"Estamos tranquilos; compartimos los comentarios del ministro que tiene que administrarse plasma en el contexto de una investigación científica, porque así lo ha hecho la gran mayoría de los países, pero consideramos que es una terapia segura", sostuvo la subdirectora de Unidades de Diagnóstico de la fundación, Carolina Selman, en entrevista con radio Universo.
Al respecto, indicó que "desde el punto de vista transfusional, nosotros seguimos los mismos criterios establecidos por el Minsal para la creación de cualquier componente sanguíneo. Por lo tanto, el plasma tiene el mismo riesgo que una transfusión de sangre para una persona que ha perdido mucha sangre por una cirugía o un accidente".
Explicó que "además, para este proyecto, le medimos anticuerpos específicos para el coronavirus y volvemos a medir con una metodología aún más sensible que la recomendada por las normas ministeriales, para VIH, Hepatitis B y Hepatitis C. Entonces, desde el punto de vista de una terapia transfusional, consideramos que es una terapia segura y extremamos las medidas para que así lo sea".
Argumentó también que "si lo vemos como un tratamiento para el coronavirus, donde no hay un tratamiento claro aún (...) y además tampoco hay una vacuna lista, consideramos que en el caso de la administración de plasma el principal beneficio es la vida del paciente porque sí hay reportes que demuestran una disminución de la mortalidad y de las complicaciones".
En ese sentido, señaló que "consideramos que es una opción concreta y válida tanto a nivel del paciente, porque vamos a disminuir la probabilidad de muerte, como a nivel general, al prevenir el colapso de los servicios de salud".
En Chile ya se utiliza en en el tratamiento del Hanta
Explicó además que "no es tan nueva la tecnología", sino que "el plasma se ha usado hace bastante tiempo en distintas pandemias, en SARS en MERS, y en Chile venimos usando el plasma desde hace un buen rato en el tratamiento del Hanta, que consiste en generar una inmunidad pasiva en los pacientes a través de la entrega de anticuerpos que vienen de una persona que ya está recuperada de la enfermedad".
"Consideramos que es un tratamiento esperanzador y seguimos trabajando con más fuerza a la espera de que el Minsal revise los nuevos antecedentes que están reportados en la literatura y cambie de parecer porque lo que queremos es trabajar juntos en beneficio de los pacientes de Chile", afirmó.
Según detalló, la terapia "consiste en que le sacamos una fracción de la sangre a un paciente, que es el plasma, que es la parte líquida de la sangre, (se extrae) de un paciente que ya tuvo la enfermedad, no importa la gravedad, pero buscamos que haya tenido una enfermedad leve, incluso buscamos asintomáticos. Le sacamos una fracción de su sangre, le hacemos todas las normas de seguridad, la alicuotamos en tres dosis y después a un paciente que cumple ciertos criterios, se le administra de una forma temprana".
El proyecto partió en marzo, cuando la FDA liberó como tratamiento de investigación el uso del plasma. "En un principio, pensamos que la técnica la íbamos a procesar solamente para pacientes oncológicos. Sin embargo, cuando empezamos a ver qué es lo que reportaba la literatura y los casos de éxito que existían, que si bien eran poquitos a principio, a medida que han ido saliendo nuevas publicaciones, se han reportado casos de hasta 5 mil pacientes, decidimos que era una terapia en la que no solamente debían estar nuestros pacientes en la FALP, sino que debíamos hacerlo a un nivel más macro", señaló.