오명돈 교수 "렘데시비르, 코로나19 회복기간 4일 단축… 표준치료제 될 것"
우리나라에서 '렘데시비르' 임상시험을 총괄한 오명돈 신종감염병 중앙임상위원회 위원장(서울대 감염내과 교수)가 렘데시비르가 코로나19 표준치료제가 될 가능성이 높다고 평가했다.
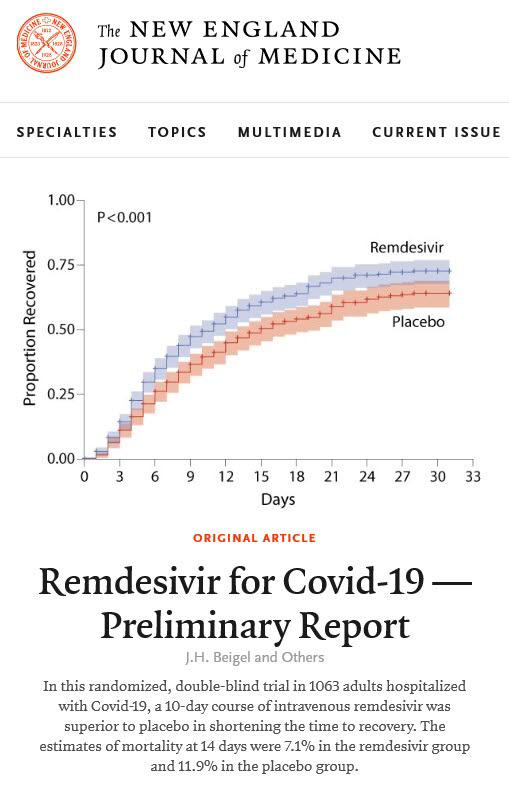
미국 국립보건연구원(NIH)가 주도한 렘데시비어 임상시험 결과가 22일(현지시간) 발표됐다. 코로나19 폐렴 환자 1063명을 대상으로 렘데시비어 또는 위약을 10일간 투여하고 위약군에 견준 결과 렘데시비르 치료군에서 회복시간이 31%(15일→11일) 단축됐다. 이 결과를 근거로 지난 1일 미국 식품의약국(FDA)은 렘데시비르를 중증환자에게 긴급사용허가를 승인했다.
이 연구는 전세계 10개국, 73개 의료기관이 참여한 다국가·다기관 임상 시험이다. 미국에서 45개 의료기관이, 유럽과 아시아에서 28개 의료기관이 참여했는데 아시아에서는 한국, 일본, 싱가포르가 참여했다. 덕분에 2월 21일 환자등록을 개시한 지 2달만에 1000명이 넘는 많은 환자를 모집할 수 있었고 이중맹검, 위약 대조 연구 디자인으로 렘데시비어의 효능을 평가할 수 있었다.
이 연구에서 2차 평가 지표는 치사율인데 치료 후 14일의 치사율은 11.9%에서 7.1%로 줄었다. 다만 치사율이 35% 감소되는 결과를 증명하려면 사망에 도달한 수가 최소 200명이 필요하고 따라서 2000여명의 시험 참가자를 모집해야 하는데 이는 팬데믹 상황에서 불가능하다고 판단해 애초 연구 디자인 단계부터 치사율 감소는 차 평가 항목에 포함되지 않았다.
대신 환자 상태가 회복되는 것을 치료의 차 평가 항목으로 설정했다. 회복이 15일에서 11일로 4일 단축됐다는 것은 인공호흡기나 중환자실, 산소와 같은 의료 자원이 그 만큼 더 많아지는 효과가 있으므로 의료 시설과 기구가 절실히 필요한 판데믹 상황에서는 매우 의미있는 효과라고 할 수 있다.
오명돈 교수는 “이번 NIH 주도 임상연구를 통해서 렘데시비르는 최초의 코로나19 치료제로 인정받게 됐다”면서 “앞으로 개발되는 코로나19치료제는 렘데시비어보다 더 월등하거나 최소한 열등하지 않다는 것을 증명해야 하는 상황이 됐다”고 설명했다.
오 교수는 “렘데시비르의 치료 효과는 아직도 개선의 여지가 남아있으며 제 2세대, 제 3세대 약물이 나올 것으로 기대한다”면서 “또 바이러스 증식 과정의 다른 부위를 타깃으로 하는 항바이러스제와 인체의 면역기능을 조절하는 약제들도 앞으로 개발될 것으로 기대한다”고 덧붙였다.
정은경 중앙방역대책본부장(질병관리본부장)은 이날 정례브리핑에서 “미국 NIH가 주관하고 다국가가 참여한 잘 디자인된 임상시험을 거쳐서 치료기간을 단축하고 또 사망률도 일부 줄일 수 있다는 유효성을 검증했다”면서 “국내에서도 긴급하게 사용에 대한 부분을 추진할 지 여부는 중앙임상위원회 쪽으로 의견을 물어보고 있는 상태이고 필요할 경우 식약처에 긴급 도입하는 부분을 요청하려고 준비를 하고 있는 상황”이라고 밝혔다.
정현정기자 iam@etnews.com